
-
Puntos de fusión y ebullición altos o muy altos (dependiendo
del valor de la energía reticular) debido a
la fortaleza del enlace iónico. Por esto todos los compuestos iónicos son
sólidos a temperatura ambiente.
- Duros (el rayarlos implica la ruptura de enlaces iónicos) pero frágiles (un golpe puede enfrentar iones del mismo signo y provocar la ruptura). ¡Pulsa el martillo!
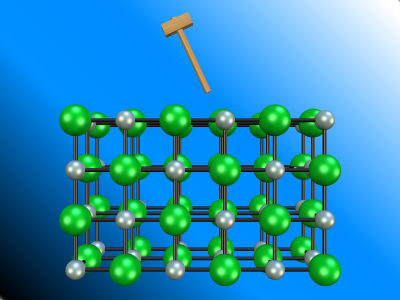
- No conducen la electricidad en estado sólido (los iones están en posiciones fijas localizadas) pero sí fundidos o disueltos (si se disuelven es en disolventes polares, de forma que el extremo negativo de las moléculas de disolvente quedará rodeando los cationes y el extremo positivo atraerá a los aniones).¡Pulsa aquí para verlo!